( الرابطة في كلوريد الصوديوم )
الرابطة في كلوريد الصوديوم

كلوريد الصوديوم هو مركب أيوني يتكون من أيونات الصوديوم (Na+) وأيونات الكلوريد (Cl-) المرتبطة معًا بواسطة رابطة أيونية قوية، حيث تتكون هذه الرابطة نتيجة انتقال إلكترون من ذرة الصوديوم إلى ذرة الكلور.
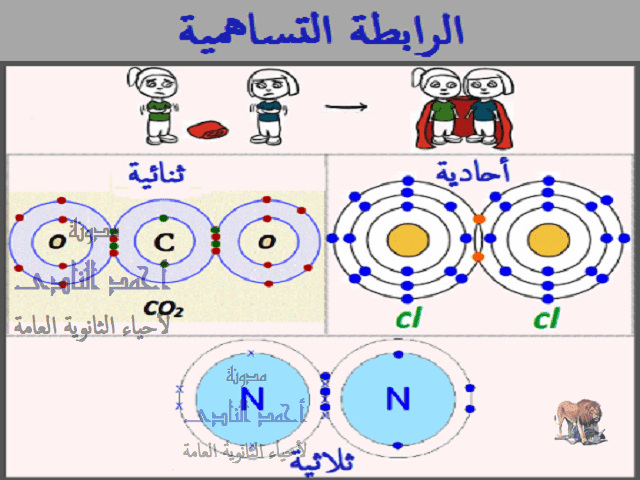
التركيب الإلكتروني لكلوريد الصوديوم
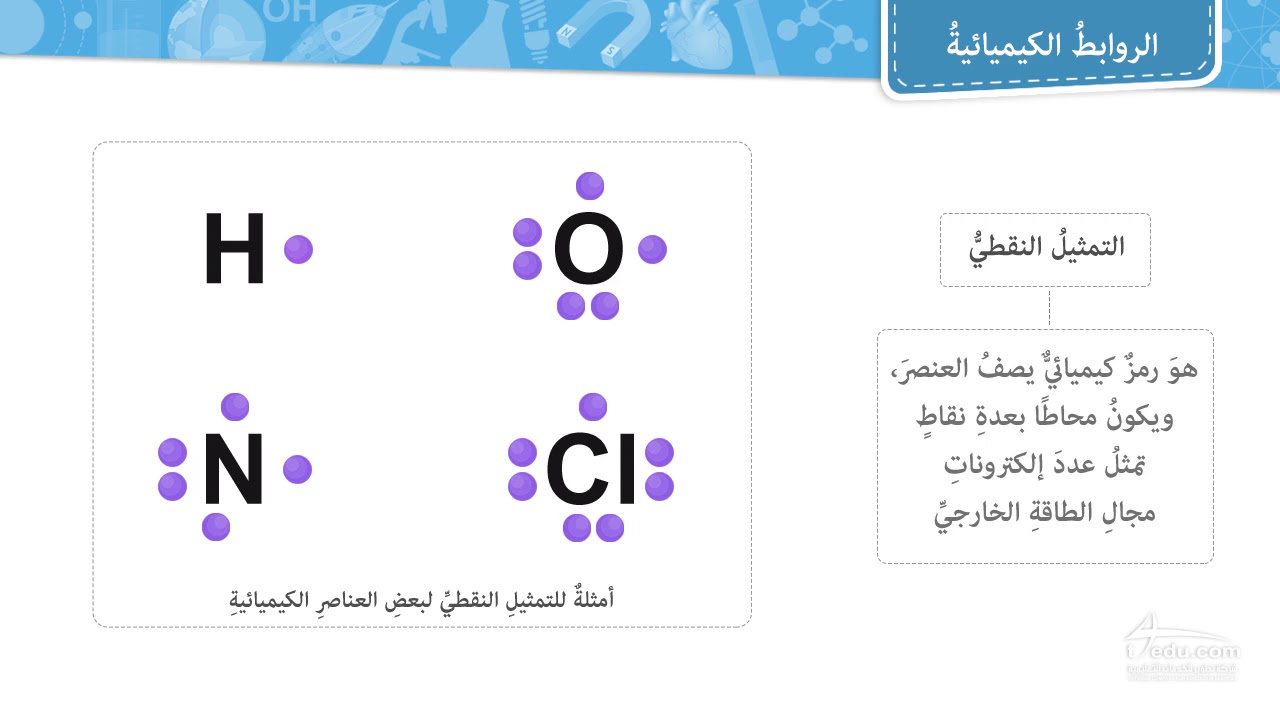
يحتوي ذرة الصوديوم على إلكترون واحد في غلافها الخارجي، والذي تميل إلى التخلي عنه بسهولة ليصبح أيون صوديوم موجب (Na+)، بينما تحتوي ذرة الكلور على سبعة إلكترونات في غلافها الخارجي، وهي بحاجة إلى إلكترون واحد لإكمال غلافها الثماني وتصبح أيون كلوريد سالب (Cl-).

عندما تتفاعل ذرتان من الصوديوم مع ذرة واحدة من الكلور، تنتقل إلكترونان من الصوديوم إلى الكلور، مما يؤدي إلى تكوين أيونين من الصوديوم وأيون واحد من الكلور.
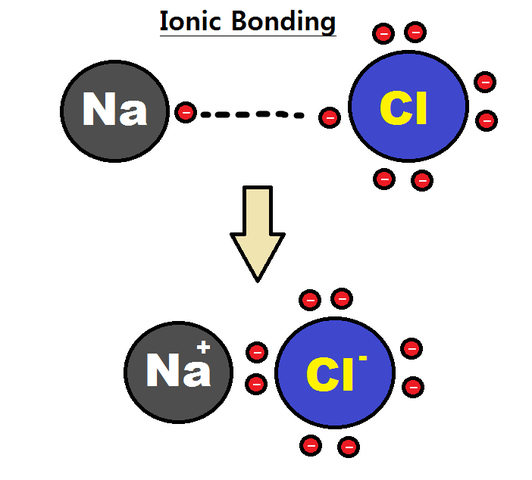
خصائص الرابطة الأيونية في كلوريد الصوديوم

- قوة الرابطة: تكون الرابطة الأيونية في كلوريد الصوديوم قوية للغاية بسبب الشحنة العالية لأيوناته، حيث يتطلب قدرًا كبيرًا من الطاقة لكسر هذه الرابطة.
- الخواص الفيزيائية: بسبب قوة الرابطة، يكون كلوريد الصوديوم مادة صلبة عالية الانصهار والغليان، كما أنه ذو كثافة عالية نسبيًا وصلابة.
- الذوبانية: كلوريد الصوديوم قابل للذوبان في الماء والمذيبات القطبية الأخرى بسبب تفاعل أيوناته مع جزيئات المذيب.
الاستخدامات الصناعية لكلوريد الصوديوم
- إنتاج الكلور والصودا: يعتبر كلوريد الصوديوم مادة خام مهمة لإنتاج غاز الكلور والصودا الكاوية، والتي تستخدم في مجموعة واسعة من الصناعات.
- صناعة الزجاج: يستخدم كلوريد الصوديوم كعامل تذويب في صناعة الزجاج، مما يساعد على خفض درجة انصهار خليط الزجاج.
- صناعة المواد الغذائية: يستخدم كلوريد الصوديوم على نطاق واسع في صناعة الأغذية كمادة حافظة ومُعزز للنكهة.
الرابطة الأيونية في كلوريد الصوديوم مقارنة بالروابط الأخرى
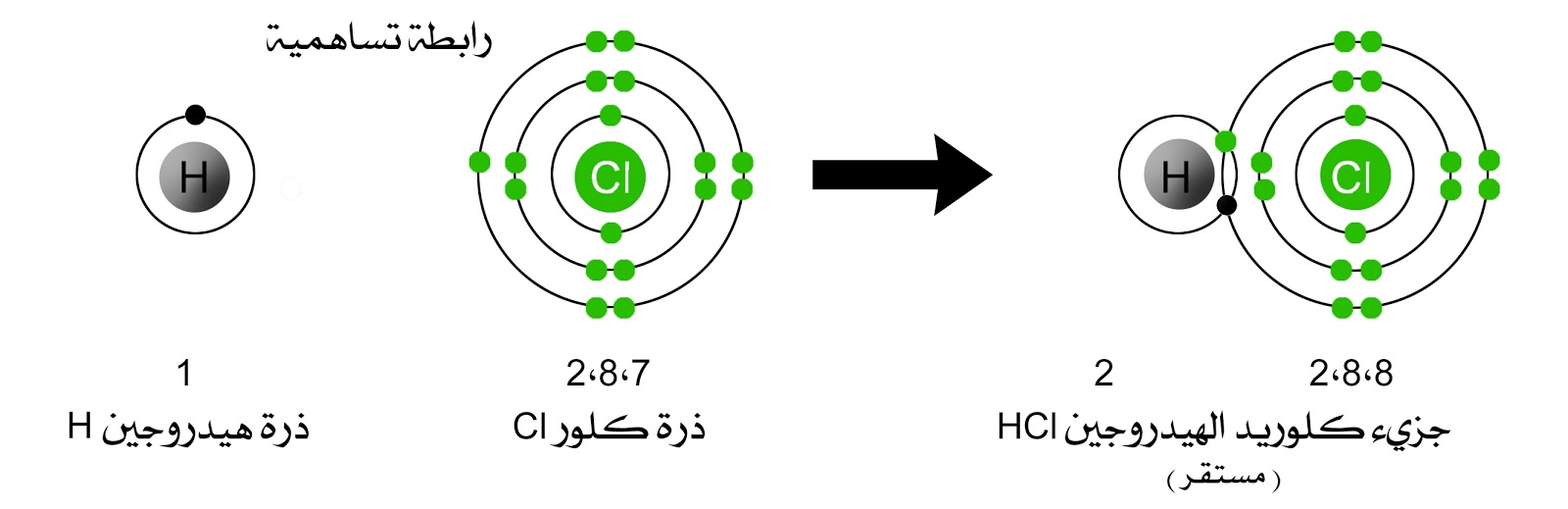
- الروابط التساهمية: على عكس الروابط الأيونية، تتشكل الروابط التساهمية عندما تشارك الذرات إلكترونات بدلاً من نقلها، مما يؤدي إلى روابط أضعف وأكثر اتجاهية.
- الروابط الفلزية: تتكون الروابط الفلزية من إلكترونات حرة تتحرك بحرية بين ذرات المعدن، مما يؤدي إلى روابط قوية ولكنها غير اتجاهية.
- روابط فان دير والس: روابط فان دير والس هي أضعف أنواع الروابط الكيميائية، وتنشأ من تفاعلات ثنائي القطب أو متعدد الأقطاب بين الجزيئات أو الذرات.
أهمية الرابطة الأيونية في كلوريد الصوديوم
- الخواص الفيزيائية الفريدة: الرابطة الأيونية القوية في كلوريد الصوديوم مسؤولة عن خواصه الفيزيائية الفريدة، مثل درجة الانصهار العالية والذوبانية في الماء.
- التفاعلات الكيميائية: تؤثر الرابطة الأيونية في كلوريد الصوديوم على تفاعلاته الكيميائية، مما يسمح له بالتفاعل مع المركبات الأخرى من خلال التبادل الأيوني.
- الأهمية البيولوجية: تلعب الروابط الأيونية في كلوريد الصوديوم دورًا مهمًا في عمليات حيوية مختلفة، مثل توازن السوائل والحفاظ على جهد الغشاء في الخلايا.
خاتمة
الرابطة الأيونية في كلوريد الصوديوم هي رابطة قوية ومتينة بين أيونات الصوديوم وأيونات الكلور، وهي مسؤولة عن الخواص الفيزيائية والكيميائية الفريدة لهذا المركب. وتلعب هذه الرابطة دورًا مهمًا في مجموعة واسعة من التطبيقات الصناعية والبيولوجية.